Arzneimittelbehörden zunehmend abhängig von Pharmagebühren (1)
Arzneimittelbehörden, die über die Zulassung von Medikamenten entscheiden, werden heute zu 50, 89 oder sogar 96 Prozent von der pharmazeutischen Industrie finanziert. Bei Gesundheitspolitikern ist dies kaum ein Thema.
Die genannten Zahlen veröffentlichte die Journalistin Maryanne Demasi kürzlich im «British Medical Journal» (BMJ). Sie bat sechs weltweit wichtige Arzneimittelbehörden (Kanada, USA, Japan, Australien, EU und Grossbritannien) um Auskunft. «Die Ergebnisse sind ernüchternd», urteilte «Der Arzneimittelbrief».
Die öffentliche Hand finanziert einen immer kleiner werdenden Anteil
Die Europäische Arzneimittelagentur EMA beispielsweise finanzierte sich noch 1995 nur zu zwanzig Prozent mit Einnahmen aus der pharmazeutischen Industrie. Im Jahr 2010 machte dieser Anteil bereits 75 Prozent aus, heute liegt er bei 89 Prozent.
Die US-Arzneimittelbehörde FDA wurde anfangs komplett durch die öffentliche Hand finanziert. 1993 erhielt sie etwa 29 Millionen Dollar an Abgaben der Pharmaindustrie. 2016 waren es 884 Millionen, also dreissigmal mehr. Aktuell kommen 65 Prozent der Einnahmen der FDA von der Pharma- und Medizinprodukteindustrie. In dem Mass, in dem die Finanzierung durch die Industrie gestiegen sei, habe auch der Input der Industrie bezüglich der Arzneimittelregulierung und -genehmigung zugenommen, heisst es in einem Artikel im «New England Journal of Medicine«.
Wie die weltweit wichtigste Arzneimittelbehörde von Gebühren abhängig wurde
Die US-amerikanische FDA ist die Arzneimittelbehörde mit dem grössten Gewicht weltweit. Ein Artikel im «New England Journal of Medicine» hat 2017 nachgezeichnet, wie diese Behörde immer mehr von den Gebühren abhängig wurde, welche die pharmazeutischen Firmen ihr bezahlen. Im Gefolge des Contergan-Skandals – die FDA hatte dieses Medikament Anfang der 1960er-Jahre nicht zugelassen – verpflichtete die FDA die Pharmafirmen ab 1962 zu Studien, um die Wirksamkeit und die Sicherheit neuer Medikamente zu belegen. Nur dann erteilte die FDA die Zulassung. Diese Neuerung führte dazu, dass sich der Begutachtungsprozess durch die FDA immer länger hinzog: Im Jahr 1963 dauerte er noch 14 Monate, 1979 über 35 Monate. Weil sie zu wenig öffentliche Gelder erhielt, konnte die FDA aber nicht mehr Mitarbeitende anstellen.
So bot die pharmazeutische Industrie in der Aids-Krise an, der FDA Gebühren zu bezahlen, damit diese im Gegenzug mehr Personal bezahlen und so den Zulassungsprozess neuer Medikamente beschleunigen konnte. 1992 hiess der US-Kongress dieses Gegengeschäft gut. Anfangs betrug die Gebühr für die Zulassung eines neuen Arzneimittels 100’000 Dollar, im Jahr 2018 waren es bereits über 2,4 Millionen Dollar. Daneben gibt es diverse weitere Gebühren.
Alle fünf Jahre muss der US-Kongress die Finanzierung der FDA über Gebühren wieder genehmigen. Hätte er das entsprechende Gesetz 2017 nicht wieder erneuert, hätten damals über 5’000 FDA-Mitarbeiter ihre Kündigung erhalten. Mit jeder Erneuerung verpflichtete sich die FDA zu bestimmten Gegenleistungen. Die pharmazeutische Industrie macht dabei jeweils auch ihre Anliegen geltend, die FDA habe zunehmend stärker darauf eingehen müssen, schrieben der Pharmakologe Aaron Kesselheim und seine Kollegen in dem Artikel. Anfangs ging es den Firmen vor allem ums Zulassungstempo. Im Jahr 2011 zum Beispiel wurden 70 Prozent der neuen Arzneimittel nach nur einer Runde im Begutachtungsprozess zugelassen, die restlichen 30 Prozent nach zwei oder mehr Runden. Drei Jahre später liess die FDA 95 Prozent der neuen Medikamente nach einer Runde zu. In den 1990er-Jahren hiess die FDA 77 Prozent der Zulassungsanträge bei neuen Arzneimitteln gut, 2017 waren es circa 86 Prozent.
Dazu trug bei, dass sich die FDA und die Firmen im Vorfeld der Zulassung viel öfter austauschen und absprechen als früher. Bei der letzten Erneuerung des Gesetzes zur Gebührenfinanzierung im Jahr 2017 verpflichtete sich die FDA, grössere Schritte zu unternehmen, um die Arzneimittelzulassung zu erleichtern. So können nun beispielsweise die Patientinnen und Patienten – deren Organisationen oft von Pharmafirmen finanziell unterstützt werden – ihre Sichtweise stärker einbringen. Ausserdem würden von der FDA mehr Flexibilität und stärkeres Eingehen auf die Bedürfnisse der Industrie verlangt, heisst es in dem Artikel.
Beim Schweizerischen Heilmittelinstitut Swissmedic stammten letztes Jahr etwa 86 Prozent des Nettoertrags aus Verfahrensgebühren und aus einer Aufsichtsabgabe, welche die Pharma- und Medizinproduktehersteller entrichten müssen. Die Aufsichtsabgabe entspricht acht Promille des Fabrikabgabepreises der in der Schweiz verkauften, zugelassenen Arzneimittel, Impfstoffe, Tierarzneimittel und Transplantatprodukte.
Swissmedic versichert, dass diese Art der Finanzierung ihre Entscheide nicht beeinflusse. Swissmedic-Mediensprecher Lukas Jaggi sagt: «Swissmedic setzt weder den Preis von Medikamenten fest, noch haben wir einen Einfluss darauf, wie viele Packungen eines Arzneimittels verkauft werden. Marktaussichten eines Arzneimittels spielen bei Zulassungsverfahren keine Rolle. Dieses Finanzierungssystem hat sich seit Jahrzehnten bewährt und es gab nie Anhaltspunkte, dass dadurch unsere Unabhängigkeit beeinflusst worden wäre.»
Die australische Wissenschaftsjournalistin Maryanne Demasi dagegen stellt einen Zusammenhang her zwischen den finanziellen Abhängigkeiten und der Geschwindigkeit und dem Wohlwollen, mit denen die Behörden Medikamente zulassen.
Die australische Arzneimittelbehörde etwa – zu 96 Prozent finanziert durch Industriegelder – hiess in den letzten beiden Jahren neun von zehn Zulassungsanträgen von Medikamenten gut. Auch diese Behörde bestreitet einen Interessenkonflikt.
Arzneimittelbehörden im Vergleich
| Land Informationen und Daten zur Behörde | Australien TGA | Europa EMA | Grossbritannien MHRA | Japan PMDA | USA FDA | Kanada HC | Schweiz Swissmedic |
|---|---|---|---|---|---|---|---|
| Budget und Gebühren | |||||||
| Anteil des Budgets, das von pharmazeutischen Unternehmen bezahlt wird | 96% | 89% | 86% | 85% | 65% | 50,5% | 86% |
| Jährliches Gesamtbudget (im Kalenderjahr 2021 oder im Fiskaljahr 2020-2021) | AU$ 170 Mio. | € 386 Mio. | £ 159 Mio. | ¥ 29,1 Mio. | US$ 6,1 Mrd. | C$ 2,7 Mrd. | CHF 123 Mio. |
| Transparenz, Interessenkonflikte | |||||||
| Anteil der Mitglieder von Covid-19 Impfkomitees mit finanziellen Interessenkonflikten † | 50 % | 3 % | 32 % | 75 % | unter 10% | 0% | 78% † |
| Erklärte Interessenkonflikte öffentlich zugänglich | Nein | Ja | Ja | Ja | Ja | Nein | Ja |
| Zulassungsbehörde erhält routinemässig die originalen Patientendaten †† | Nein | Nein | Nein | Ja | Ja | Nein | Nein |
| Arzneimittelzulassungen | |||||||
| Neue Arzneimittel: Anteil positiver Zulassungsbescheide im Verhältnis zu den negativen Bescheiden | 94% | 88% | 98,5% | nicht offengelegt | 69%* 29%** | 83% | 100% *** |
| Anteil neuer Arzneimittel mit beschleunigter Zulassung im Jahr 2020 | 20% | 50% | 36% | 26% | 68% | 16% | 56% |
«Sie halten Daten zurück»
US-Soziologe Donald Light, der sich jahrzehntelang mit der Medikamentenzulassung beschäftigte, erklärte im «BMJ»: Die Arzneimittelbehörden «sind nicht rigoros, sie sind nicht unabhängig, sie sind selektiv und sie halten Daten zurück. Ärzte und Patienten müssen begreifen, wie tiefgreifend und umfassend man den Arzneimittelbehörden nicht trauen kann, solange sie von der Industrie finanziert werden.»
Vier der sechs von Demasi angefragten Arzneimittelbehörden werten Patientendaten aus den Medikamentenstudien nicht selbst aus. Nur zwei der sechs Behörden, die FDA und die japanische PMDA, hätten überhaupt die Rohdaten der Studienteilnehmenden, sie würden diese aber nicht «proaktiv» veröffentlichen. Die FDA sperrte sich jüngst sogar dagegen, Rohdaten der grossen Covid-Impfstudie von Pfizer/Biontech herauszugeben (Infosperber berichtete).
Die australische Behörde musste auf ein Gesuch hin offen legen, dass sie bei den Covid-Impfstudien über die Datensätze zu den einzelnen Patienten nicht verfüge. Sie räumte auch ein, dass sie bei den Covid-Impfungen die Originaldaten nicht gesehen hatte. Stattdessen prüfte und beurteilte sie vornehmlich die Daten, welche die Hersteller «aggregiert oder gepoolt» hatten.
Swissmedic stützte sich laut Mediensprecher Lukas Jaggi bei der Begutachtung der Zulassungsgesuche für die Covid-19-Impfstoffe ebenfalls auf die von den Herstellern gelieferten, gepoolten Daten und betrachtete bei Bedarf einzelne Rohdaten.
Es sei theoretisch möglich, dass von Herstellern auch Studien gemacht würden, die der Behörde nicht eingereicht würden, sagt Jaggi.
Swissmedic hat beim Zulassungstempo die Europäische Behörde überholt
Von den etwa 500 Mitarbeitenden (rund 430 Vollzeitstellen) bei Swissmedic sind circa 170 Personen für die Medikamentenzulassung tätig. Sie haben im Jahr 2021 insgesamt 45 neue Humanarzneimittel zugelassen, darunter zwei Covid-Impfstoffe und ein Medikament gegen Covid-19. Etwa 30 Personen sind laut Swissmedic-Sprecher Lukas Jaggi fürs Überwachen der Arzneimittelsicherheit zuständig. Insgesamt sind über 5’700 Arzneimittel für Menschen in der Schweiz zugelassen, mehr als 12’000 Komplementärarzneimittel, 14 Transplantatprodukte und 693 Medikamente für Tiere.
Bei den Zulassungsgesuchen für neue Medikamente stünden die Behörden verschiedener Länder untereinander in einem gewissen Wettbewerbsverhältnis, sagt Swissmedic-Sprecher Lukas Jaggi. Die Schweizer Behörde erhalte Zulassungsgesuche von den Firmen und auch Antworten auf gestellte Fragen zum Teil später als die FDA. Laut einem «Benchmarking«, das Swissmedic zusammen mit etlichen pharmazeutischen Firmen durchführt, wurden Zulassungsgesuche bei Swissmedic im Durchschnitt 322 Tage später eingereicht als bei der «Referenzbehörde» FDA.
Beim Begutachtungstempo hat Swissmedic in den letzten beiden Jahren zugelegt. «Es soll für die Firmen attraktiv sein, ein Zulassungsgesuch bei uns einzureichen», sagt Jaggi.
«Swissmedic ist verpflichtet, ihren Prozess der Evaluierung von Arzneimitteln ständig zu optimieren und zu straffen», heisst es in einer Analyse, die zwei Swissmedic-Mitarbeiter und Kolleginnen 2019 publiziert haben. Diese Feststellung dürfte für alle wichtigen Arzneimittelbehörden zutreffen.
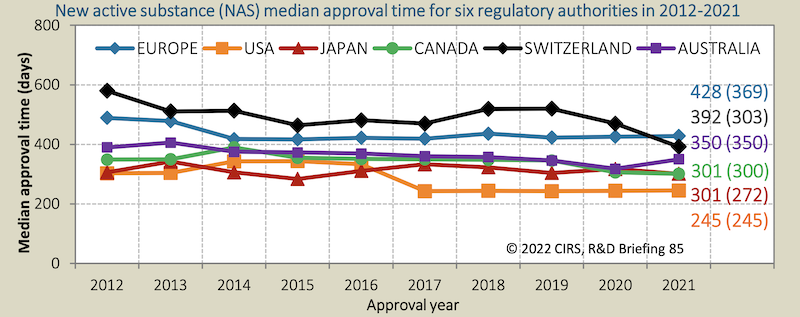
2019 benötigte Swissmedic laut dem «Centre for Innovation in Regulatory Science» im Mittel noch rund 500 Tage fürs Prüfen eines Medikamenten-Zulassungsantrags. Im Jahr 2021 dauerte es vom Einreichen eines Gesuchs bis zur Zulassung im Mittel 392 Tage (147 Tage länger als bei der FDA). Damit unterbot Swissmedic erstmals die europäische Arzneimittelbehörde EMA (428 Tage im Mittel).
In der Schweiz habe das Abfassen der Arzneimittelinformationen früher viel Zeit in Anspruch genommen, sagt Jaggi. «Dieser Prozess ging viel zu lange. Vor allem in diesem Bereich haben wir in den letzten Jahren gezielt Massnahmen ergriffen und im letzten Jahr erfreuliche Beschleunigungen erreicht.»
Zunehmend häufiger arbeitet Swissmedic mit den Behörden anderer Länder zusammen. Dabei werden Aufgaben aufgeteilt, am Ende trifft aber jede Behörde ihren eigenen Entscheid. Dieses Vorgehen soll Prozesse beschleunigen und die Begutachtungsqualität erhöhen.
Swissmedic verweist auf eine Analyse, die im Fachblatt «Therapeutic Innovation & Regulatory Science» erschienen ist. Dort verglichen zwei Swissmedic-Mitarbeiter und weitere Wissenschaftlerinnen die Zulassungsentscheide von Swissmedic mit denen der US-Behörde FDA und der europäischen EMA in den Jahren 2005 bis 2014. Veröffentlicht wurde ihre Analyse fünf Jahre später.
Von 255 neuen Medikamenten, die damals von allen drei Behörden unabhängig voneinander geprüft wurden, hiess die EMA 91 Prozent der Zulassungsgesuche gut, die FDA 87 Prozent und Swissmedic 84 Prozent.
Auch politische Prioritäten können den Ausschlag geben
Ein Grund für die Unterschiede könnte laut der Studie sein, dass die Hersteller Zulassungsanträge bei Swissmedic tendenziell später einreichen würden als bei der FDA oder der EMA. Da die Hersteller bis zum Antrag noch weitere Studiendaten sammeln, erhalte Swissmedic so umfassendere Daten als die anderen beiden Behörden. Ein anderer Grund könne die engere Zusammenarbeit zwischen der FDA und den Herstellern bei beschleunigten Zulassungsverfahren sein. Werde die Behörde bereits bei den für die Zulassung nötigen Studien stärker eingebunden, gehe dies mit einer höheren Zulassungsquote einher.
In 90 von 100 Fällen kam Swissmedic zwischen 2005 und 2014 zum selben Schluss wie die EMA, in 85 von 100 Fällen stimmten die Entscheide von Swissmedic mit denen der FDA überein. In einem von fünf Fällen – das betraf 50 Zulassungsgesuche – gingen die Ansichten der drei Behörden jedoch auseinander.
«Nicht zuletzt können kulturelle, politische, rechtliche sowie länderspezifische gesundheitliche Prioritäten im Einzelfall den Ausschlag für eine Zulassung oder Ablehnung gegeben haben. Die Beurteilung von Nutzen und Risiko eines Arzneimittels ist keine exakte Wissenschaft, sondern hängt bis zu einem gewissen Grad auch von den Persönlichkeiten und Hintergründen der an der Beurteilung beteiligten Kollegen ab.»
Zitat aus der Studie zum Vergleich von Swissmedic, FDA und EMA, «Therapeutic Innovation & Regulatory Science» 2019
«Interne Meinungsführer» und «unbewusstes Gruppendenken»
Auch wenn sich alle drei Behörden mittels beigezogener externer Experten und Gutachter um einen ausgewogenen Entscheidungsprozess bemühten, sei «ein subjektives Element im Evaluationsprozess» nicht auszuschliessen. Zum Beispiel könne es vorkommen, dass «‹interne Meinungsführer› mit einem gewissen Ansehen innerhalb ihrer jeweiligen Organisation» oder «unbewusstes Gruppendenken» die Entscheide beeinflussen würden.
Von den Produkten, bei denen nur eine der drei Arzneimittelbehörden ein Zulassungsgesuch guthiess, während die anderen beiden es zurückwiesen, wurden später fast 19 Prozent später wieder vom Markt genommen. Bei den Arzneimitteln, bei denen sich alle drei Behörden einig waren mit der Zulassung, wurden hingegen nur knapp vier Prozent aus dem Verkehr gezogen.
Bezogen auf 280 zugelassene Produkte sei die Marktrücknahme von 16 zwar wenig, aber «dennoch bemerkenswert, wenn man die potenziellen gesundheitlichen Folgen bedenkt, die mit der Rücknahme eines Arzneimittels verbunden sind», schreiben die Autoren. In vier der 16 Fälle führten Sicherheitsbedenken zum Rückzug, in fünf Fällen war der Grund unklar und sieben Mal waren kommerzielle Gründe ausschlaggebend.
Themenbezogene Interessenbindung der Autorin/des Autors
Keine
_____________________
Meinungen in Beiträgen auf Infosperber entsprechen jeweils den persönlichen Einschätzungen der Autorin oder des Autors.










Bis zum neuen Heilmittelgesetz 2001 hat die Zulassungsbehörde die CH-Preise «geschützt» und Preissenkungen praktisch verboten. Es brauchte die Intervention der Wettbewerbsbehörden, um die Trennung zw. gesundheitlichen und kommerziellen Aspektes des Medikamentenmarktes auch institutionell durchzusetzen.
Vgl z.B. zur Entwicklung des CH-Pharmamarktes und insbesondere der reglementarischen Rahmenbedingungen bis 2007
https://www.preisueberwacher.admin.ch/dam/pue/de/dokumente/studien/medikamentenpreiseundmedikamentenmarktinderschweiz.pdf.download.pdf/medikamentenpreiseundmedikamentenmarktinderschweiz.pdf
Zur Entwicklung der Zulassungsprozedere vgl.
https://biblio.parlament.ch/e-docs/375517.pdf